Pfizer Εγκλήματα κατά των παιδιών μας: Καρδιακή ανακοπή μωρού δύο μηνών μια ώρα μετά το πειραματικό εμβόλιο. 58 μωρά που έλαβαν mRNA εμβόλια COVID-19 υπέστησαν απειλητικές για τη ζωή ανεπιθύμητες ενέργειες

Όλα τα άρθρα της Global Research μπορούν να διαβαστούν σε 51 γλώσσες ενεργοποιώντας το αναπτυσσόμενο μενού «Μετάφραση Ιστότοπου» στο επάνω banner της αρχικής μας σελίδας (έκδοση για υπολογιστές)….
Για να λάβετε το Daily Newsletter της Global Research (επιλεγμένα άρθρα), κάντε κλικ εδώ .
Ακολουθήστε μας στο Instagram και στο Twitter και εγγραφείτε στο κανάλι μας στο Telegram . Μη διστάσετε να αναδημοσιεύσετε και να μοιραστείτε ευρέως άρθρα της Παγκόσμιας Έρευνας.
Δημοσιεύθηκε για πρώτη φορά στις 17 Ιουλίου 2022
Σημείωση του συντάκτη της παγκόσμιας έρευνας
Διαβάστε προσεκτικά. Η Pfizer διαπράττει εγκλήματα κατά της ανθρωπότητας, ειδικά κατά των παιδιών μας.
Το εμβόλιο οδήγησε σε καρδιακή ανακοπή όχι σε ένα ηλικιωμένο άτομο αλλά σε ένα μωρό δύο μηνών.
«Γιατί δεν παρακολούθησαν την κατάσταση του μωρού 2 μηνών, αφού έπαθε καρδιακή ανακοπή μία ώρα μετά τη λήψη του πειραματικού εμβολίου; Γιατί δεν υπάρχουν περισσότερες πληροφορίες; Μήπως επειδή πέθανε; Ή αφαιρέθηκε το μωρό από ένα πείραμα; Γιατί ο συντάκτης της έκθεσης δεν το αναφέρει αυτό;»
Καλούμε το Υπουργείο Δικαιοσύνης των ΗΠΑ να αναλάβει ποινική έρευνα κατά της Pfizer.
Καλούμε τις κυβερνήσεις σε όλο τον κόσμο να αναστείλουν αμέσως το εμβόλιο mRNA.
Απαιτείται επίσης μήνυση ομαδικής αγωγής για λογαριασμό των εκατοντάδων χιλιάδων θυμάτων του εμβολίου mRNA.
Δεν αναφέρθηκε ποτέ από τα μέσα ενημέρωσης, η Pfizer έχει ποινικό μητρώο με το Υπουργείο Δικαιοσύνης των ΗΠΑ.
Το 2009 η Pfizer κατηγορήθηκε για «δόλιο μάρκετινγκ».
Michel Chossudovsky , Global Research, 6 Αυγούστου 2022
***
Δημοσιεύτηκε για πρώτη φορά από το globalresearch.ca στις 6 Ιουλίου 2022
***
Μια ανάλυση των εκθέσεων VAERS δείχνει ότι σε αντίθεση με το ενημερωτικό έγγραφο της FDA που ισχυρίζεται ότι η πλειονότητα των ανεπιθύμητων ενεργειών στην κλινική δοκιμή της Pfizers δεν ήταν σοβαρές – τουλάχιστον 58 περιπτώσεις απειλητικών για τη ζωή παρενεργειών σε βρέφη κάτω των 3 ετών που έλαβαν εμβόλια mRNA αναφέρθηκαν. Για κάποιους, δεν είναι σαφές αν επέζησαν. Δεν είναι επίσης σαφές γιατί τα βρέφη εμβολιάστηκαν και αν συμμετείχαν στις κλινικές δοκιμές. Ωστόσο, στην επικείμενη συνεδρίαση του FDA την Τετάρτη, ο FDA δεν θα μπορεί να υποστηρίξει ότι δεν γνώριζε
“Πόνος στο στήθος; καρδιακό επεισόδιο; Δέρμα ψυχρό μαλακό». Αυτή η σύντομη περιγραφή μιας καρδιακής ανακοπής, η οποία συνέβη μία ώρα μετά τη λήψη ενός εμβολίου Pfizer-BioNTech για τον COVID-19, προέρχεται από το σύστημα VAERS – το Σύστημα Αναφοράς Ανεπιθύμητων Εμβολίων των ΗΠΑ ( αριθμός περίπτωσης 1015467 ) και δεν αναφέρεται σε ηλικιωμένος, ούτε σε νεαρό ενήλικα, ή ακόμα και έφηβο. Είναι δύσκολο να πιστέψει κανείς, αλλά αυτή η αναφορά αναφέρεται σε ένα μωρό δύο μηνών .
“Ένας αρσενικός ασθενής 2 μηνών έλαβε bnt162b2 (PFIZER-BioNTech COVID-19 VACCINE) αριθμός παρτίδας: EL 739, μέσω απροσδιόριστης οδού χορήγησης στις 02 Φεβρουαρίου 2021 σε εφάπαξ δόση για ανοσοποίηση κατά του COVID-19”, όπως αναφέρεται στην κανω ΑΝΑΦΟΡΑ. «Ο ασθενής υποβλήθηκε σε εμβολιασμό, παρατηρήθηκε για 15 λεπτά έφυγε από την κλινική και επέστρεψε μία ώρα αργότερα στις 02 Φεβρουαρίου 2021, παρουσιάζοντας ως δέρμα ψυχρό, βρώμικο και με πόνο στο στήθος, αναπτύχθηκε επεισόδιο καρδιακής ανακοπής, ο ασθενής σταθεροποιήθηκε και μεταφέρθηκε για περαιτέρω ιατρική θεραπεία… Το αποτέλεσμα των γεγονότων ήταν άγνωστο. Αυτό το κρούσμα αναφέρθηκε ως σοβαρό με κριτήρια σοβαρότητας-απειλητικό για τη ζωή από HA. Δεν είναι δυνατές προσπάθειες παρακολούθησης. Δεν αναμένονται περισσότερες πληροφορίες».
Πώς ένα μωρό 2 μηνών έλαβε το εμβόλιο mRNA; Αυτά τα εμβόλια δεν έχουν λάβει ακόμη EUA (Έγκριση Χρήσης Έκτακτης Ανάγκης) για εγκεκριμένη χρήση σε παιδιά ηλικίας πέντε ετών και κάτω από τον FDA ή οποιαδήποτε άλλη ρυθμιστική αρχή, και ακόμη κι αν λάβει, η EUA θα περιλαμβάνει μόνο μωρά 6 μηνών και άνω.
Αυτό το μωρό συμμετείχε στις κλινικές δοκιμές της Pfizer-BioNTech, δοκιμάζοντας την αποτελεσματικότητα και την ασφάλεια μεταξύ των μωρών;
Η απάντηση είναι ασαφής. Σύμφωνα με το άτομο που έγραψε την αναφορά «Δεν είμαι σίγουρος αν ο ασθενής είχε εγγραφεί σε κλινική δοκιμή». Ωστόσο, ο συντάκτης της αναφοράς δηλώνει επίσης ότι η αναφορά ” λήφθηκε από έναν Άλλο Επαγγελματία Υγείας με δυνατότητα επικοινωνίας από την Pfizer από τον Ρυθμιστικό Οργανισμό” . Αυτό το σημείωμα υπονοεί ότι το βρέφος μπορεί να συμμετείχε πράγματι στη δίκη της Pfizer. Η αναφορά του ρυθμιστικού φορέα Αναφορά ασφάλειας Μοναδικό αναγνωριστικό GB-MHRA-ADR 24687611 – υποδεικνύει ότι η αναφορά προήλθε από τη Μεγάλη Βρετανία (τα πρώτα 2 γράμματα στο αναγνωριστικό αναφοράς αντιπροσωπεύουν τη χώρα προέλευσης, GB- Μεγάλη Βρετανία και MHRA ότι η πηγή της αναφοράς ήταν η αρχή της για τα ναρκωτικά).
Γιατί δεν παρακολούθησαν την κατάσταση του μωρού 2 μηνών, αφού έπαθε καρδιακή ανακοπή μία ώρα μετά τη λήψη του πειραματικού εμβολίου; Γιατί δεν υπάρχουν περισσότερες πληροφορίες; Μήπως επειδή πέθανε; Ή αφαιρέθηκε το μωρό από ένα πείραμα; Γιατί ο συντάκτης της έκθεσης δεν το αναφέρει αυτό;
Συγκλονιστικά, αποδεικνύεται ότι αυτό το περιστατικό δεν είναι μεμονωμένο, αλλά στην πραγματικότητα ένα από τα πολλά στο σύστημα VAERS, που περιγράφει μωρά και παιδιά κάτω των πέντε ετών που εκτέθηκαν σε εμβόλια mRNA Covid, τα οποία υπέστησαν απειλητικές για τη ζωή ανεπιθύμητες ενέργειες.
Παρόλο που τα παιδιά κάτω των πέντε ετών δεν θεωρούνταν κατάλληλα για αυτά τα εμβόλια εκτός και αν ήταν μέρος μιας κλινικής δοκιμής, εκπληκτικά, φαίνεται ότι υπάρχουν πολλές αναφορές στο σύστημα που περιγράφουν μωρά και νήπια που εμβολιάστηκαν. Μερικά από τα παιδιά υπέφεραν από ανεπιθύμητες ενέργειες απειλητικές για τη ζωή. Σε ορισμένες περιπτώσεις, δεν είναι σαφές τι τους συνέβη. επιβίωσαν και ανέρρωσαν, υποφέρουν ακόμα από προβλήματα υγείας ή πέθαναν.
Σε λίγες μέρες, στις 15 Ιουνίου, η Συμβουλευτική Επιτροπή Εμβολίων και Συναφών Βιολογικών Προϊόντων του FDA θα συζητήσει τα αιτήματα EUA της Moderna και της Pfizer για εμβόλια για βρέφη και νήπια ηλικίας 6 μηνών έως 4 ετών – η μόνη ομάδα που δεν είναι ακόμη κατάλληλη για εμβολιασμό κατά του COVID-19 σήμερα.
Σύμφωνα με το ενημερωτικό έγγραφο του FDA που κυκλοφόρησε σήμερα ενόψει της συνεδρίασης των επιτροπών VRBPA, υπήρξαν «245 αναφορές των ΗΠΑ» στο σύστημα VAERS «σε παιδιά ηλικίας 6 μηνών έως 4 ετών», στα οποία χορηγήθηκαν ενέσεις («προϊόν που χορηγήθηκε σε ασθενή με ακατάλληλο ηλικία» ή «χρήση εκτός ετικέτας») ή έκθεση στο εμβόλιο «μέσω μητρικού γάλακτος». Ωστόσο, και οι δύο εταιρείες ανακοίνωσαν ήδη τον Μάιο ότι τα ευρήματά τους δείχνουν ότι τα εμβόλια τους είναι ασφαλή και αποτελεσματικά.
Το Ενημερωτικό Έγγραφο του VRBPAC παραθέτει μια ποικιλία ανεπιθύμητων ενεργειών που αναφέρθηκαν μετά την έκθεση στο εμβόλιο σε αυτήν την ηλικιακή ομάδα, όπως «πυρεξία…, θερμοκρασία σώματος…, βήχας, πονοκέφαλος, εξάνθημα, διάρροια» . Σύμφωνα με το έγγραφο, «Μεταξύ των αναφορών VAERS των ΗΠΑ για άτομα ηλικίας 6 μηνών έως 4 ετών, που μπορεί να αντικατοπτρίζουν μη εξουσιοδοτημένη χρήση του εμβολίου ή μπορεί να αντικατοπτρίζουν σφάλμα αναφοράς, η πλειονότητα (96,3%) ήταν μη σοβαρές».
Ενώ το έγγραφο προσδιορίζει ανησυχίες για την ασφάλεια που εντοπίστηκαν από δεδομένα επιτήρησης ασφάλειας μετά την έγκριση στο VAERS, συμπεριλαμβανομένης της αναφυλαξίας, της μυοκαρδίτιδας και της περικαρδίτιδας, δεν σχετίζεται με αυτές τις ανησυχίες για την ασφάλεια που εντοπίστηκαν στη νεότερη ηλικιακή ομάδα. Αντίθετα, αναφέρει: «Δεν εντοπίστηκαν ασυνήθιστη συχνότητα, ομάδες ή άλλες τάσεις για ανεπιθύμητα συμβάντα που να υποδηλώνουν νέα ανησυχία για την ασφάλεια».
Είναι όμως πράγματι έτσι; Φαίνεται ότι ανεξάρτητα από τα αποτελέσματα, και παρά τα ανησυχητικά και συγκλονιστικά ευρήματα που αποκαλύπτονται από τα έγγραφα της Pfizer, αναμένεται ότι και οι δύο εταιρείες θα λάβουν το επιθυμητό EUA πολύ σύντομα. Μάλιστα, η ιστοσελίδα του CDC, ήδη τον Απρίλιο, είχε διαφημίσει ένα πρωτόκολλο σχετικά με τον εμβολιασμό των παιδιών , το οποίο περιελάμβανε και μωρά 6 μηνών έως 4 ετών.
Υπό το φως αυτής της αναμενόμενης έγκρισης, το RT Magazine διεξήγαγε μια ανάλυση των περιπτώσεων που αναφέρθηκαν στο σύστημα VAERS και αφορούσαν μωρά έως 3 ετών.
Κατά τη διάρκεια της ανάλυσης αφαιρέθηκαν περιπτώσεις στις οποίες αναφέρθηκε ότι η έκθεση στο εμβόλιο ήταν μέσω του θηλασμού (αυτές οι περιπτώσεις αναλύθηκαν χωριστά και σύντομα θα παρουσιαστούν σε επόμενο άρθρο), καθώς και περιπτώσεις που εντοπίστηκαν ως λάθη στο την εγγραφή ηλικίας.
Η ανάλυση δείχνει ότι υπήρχαν τουλάχιστον 58 περιπτώσεις σοβαρών και απειλητικών για τη ζωή ανεπιθύμητων ενεργειών μεταξύ μωρών και νηπίων 3 ετών και κάτω. Αυτό το εύρημα είναι ιδιαίτερα αινιγματικό, λαμβάνοντας υπόψη το γεγονός ότι δεν έπρεπε να εμβολιαστούν σε αυτή την ηλικία εξαρχής. Δυστυχώς, όπως και στην περίπτωση που αναφέρθηκε παραπάνω, οι περισσότερες αναφορές VAERS δεν αναφέρουν πώς και υπό ποιες συνθήκες εκτέθηκαν στο εμβόλιο – συμμετείχαν στις δοκιμές των εταιρειών; Και αν όχι, γιατί και υπό ποιες συνθήκες εμβολιάστηκαν;
Και οι δύο εταιρείες δεν έχουν ακόμη δημοσιεύσει τα δεδομένα ασφάλειας από τις δοκιμές τους σε αυτήν την ηλικιακή ομάδα. Ωστόσο, ένα πράγμα είναι σαφές από τις αναφορές VAERS: υπήρχαν πολλά μωρά που τραυματίστηκαν μετά τη λήψη του εμβολίου. Είτε εμβολιάστηκαν στις δοκιμές είτε παράνομα στις κοινότητές τους, η Pfizer και η Moderna δεν θα είναι προκλητικά σε θέση να ισχυριστούν, όταν παρουσιάζουν τα δεδομένα τους στον FDA, ότι το εμβόλιο είναι ασφαλές για μωρά,και ότι δεν υπήρξαν σοβαρές ανεπιθύμητες ενέργειες σε αυτήν την ηλικιακή ομάδα. Επιπλέον, οι εμπειρογνώμονες της επιτροπής FDA που θα συζητήσουν την έγκριση EUA δεν θα μπορούν να αγνοήσουν αυτές τις περιπτώσεις και να υποστηρίξουν ότι δεν γνώριζαν. Τα δεδομένα που παρουσιάζονται σε αυτό το άρθρο καταδεικνύουν χωρίς καμία αμφιβολία το εντελώς αντίθετο, και αυτή τη φορά – αυτά τα δεδομένα παρουσιάζονται στο κοινό εκ των προτέρων, πριν από τη χορήγηση του EUA και πριν από τη συζήτηση για το VRBPAC.
Η έκβαση των γεγονότων: Δεν ανέκαμψε
Μία από τις πιο ανατριχιαστικές αναφορές αναφέρεται σε ένα θηλυκό μωρό 43 ημερών, το οποίο στις 30 Ιανουαρίου 2021 έλαβε το εμβόλιο Pfizer’s Comirnaty. Στην περιγραφή του περιστατικού (αρ. αναφοράς 1133837) αναφέρεται ξεκάθαρα ότι ήταν εμβολιασμένη και ότι το εμβόλιο έγινε ένεση στον μυ: «Μια γυναίκα ασθενής 43 ημερών έλαβε bnt162b2 (COMIRNATY), ενδομυϊκά στις 30 Ιανουαρίου 2021 (Αριθμός παρτίδας: EK9788) ως ΜΟΝΑΔΙΚΗ ΔΟΣΗ για ανοσοποίηση κατά του COVID-19» . Αμέσως μετά τον εμβολιασμό, το μωρό υπέστη μια ποικιλία απειλητικών για τη ζωή πολυσυστημικών τραυματισμών, όπως π.χ.«Αναφυλακτική αντίδραση (ευρεία), Άσθμα/βρογχόσπασμος (στενός), Αντιχολινεργικό σύνδρομο (ευρεία), Οξεία κεντρική αναπνευστική καταστολή (ευρεία), Πνευμονική υπέρταση (ευρεία), Καρδιομυοπάθεια (ευρεία), Ηωσινοφιλική πνευμονία (ευρεία), Αιθουσαία Διαταραχές (ευρεία) , Υπερευαισθησία (ευρεία), Αναπνευστική ανεπάρκεια (στενή), Φαρμακευτική αντίδραση με ηωσινοφιλία και σύνδρομο συστηματικών συμπτωμάτων (ευρεία) ». Αν και στην ενότητα που αναφέρει το θάνατο η δήλωση δηλώνει “Όχι”, η ενότητα που αναφέρει την ανάκτηση αναφέρει επίσης “Όχι” – που σημαίνει ότι το μωρό δεν έχει αναρρώσει. Τι της συνέβη τότε; Ζει ή πέθανε;
Επιπλέον, αυτή η έκθεση, όπως και πολλές άλλες, εγείρει μερικά δύσκολα ερωτήματα. Πώς ένα μωρό 43 ημερών έλαβε ένα εμβόλιο που δεν έχει ακόμη εγκριθεί για χρήση σε μωρά; Επιπλέον, οι τρέχουσες κλινικές δοκιμές που διεξάγονται υποτίθεται ότι περιλαμβάνουν μωρά και παιδιά άνω των 6 μηνών. Αυτό το μωρό συμμετείχε στη δίκη της Pfizers; Η έκθεση δεν απαντά σε αυτό το ερώτημα.
Ακριβώς όπως αυτό το μωρό, αποδεικνύεται ότι στις περισσότερες από τις αναφερόμενες περιπτώσεις καταγράφηκαν αρκετές απειλητικές για τη ζωή ανεπιθύμητες ενέργειες για το ίδιο μωρό. Οι πιο συχνές σοβαρές ανεπιθύμητες ενέργειες ήταν η επικίνδυνη αιμορραγία. αναφυλακτικό σοκ – μια απειλητική για τη ζωή αλλεργία που μπορεί να βλάψει το αναπνευστικό σύστημα και να προκαλέσει ζάλη, λιποθυμία, ακόμη και θάνατο. αντιχολινεργικό σύνδρομο- μια κατάσταση που εμφανίζεται όταν οι θέσεις των υποδοχέων για τον νευροδιαβιβαστή ακετυλοχολίνη είναι αποκλεισμένοι, γεγονός που μπορεί να οδηγήσει σε προβλήματα συντονισμού, αυξημένο καρδιακό ρυθμό και άλλα συμπτώματα. εγκεφαλίτιδα – εγκεφαλική λοίμωξη, που μπορεί να προκαλέσει πονοκεφάλους, έμετο, απώλεια συνείδησης και θάνατο. υπογλυκαιμία – πολύ χαμηλό σάκχαρο στο αίμα, μια κατάσταση που μπορεί γρήγορα να κλιμακωθεί σε θάνατο στα βρέφη. και το νευροληπτικό σύνδρομο – το οποίο είναι επίσης απειλητικό για τη ζωή και μπορεί να βλάψει τους καρδιακούς μυς, άλλους μύες,
Από τη σύνοψη των ευρημάτων της ανάλυσης ανάλογα με την ηλικία και τις ομάδες φύλου προκύπτει η ακόλουθη εικόνα:
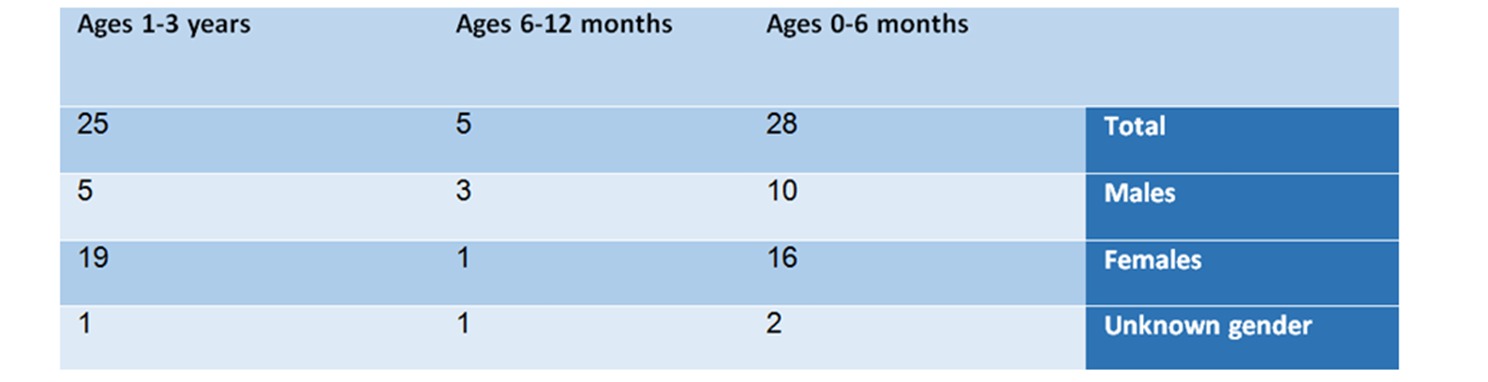
Στην ηλικιακή ομάδα 0-6 μηνών – υπάρχουν 28 αναφορές, στις οποίες οι 10 είναι άνδρες, οι 16 είναι γυναίκες και οι 2 των οποίων το φύλο δεν προσδιορίστηκε.
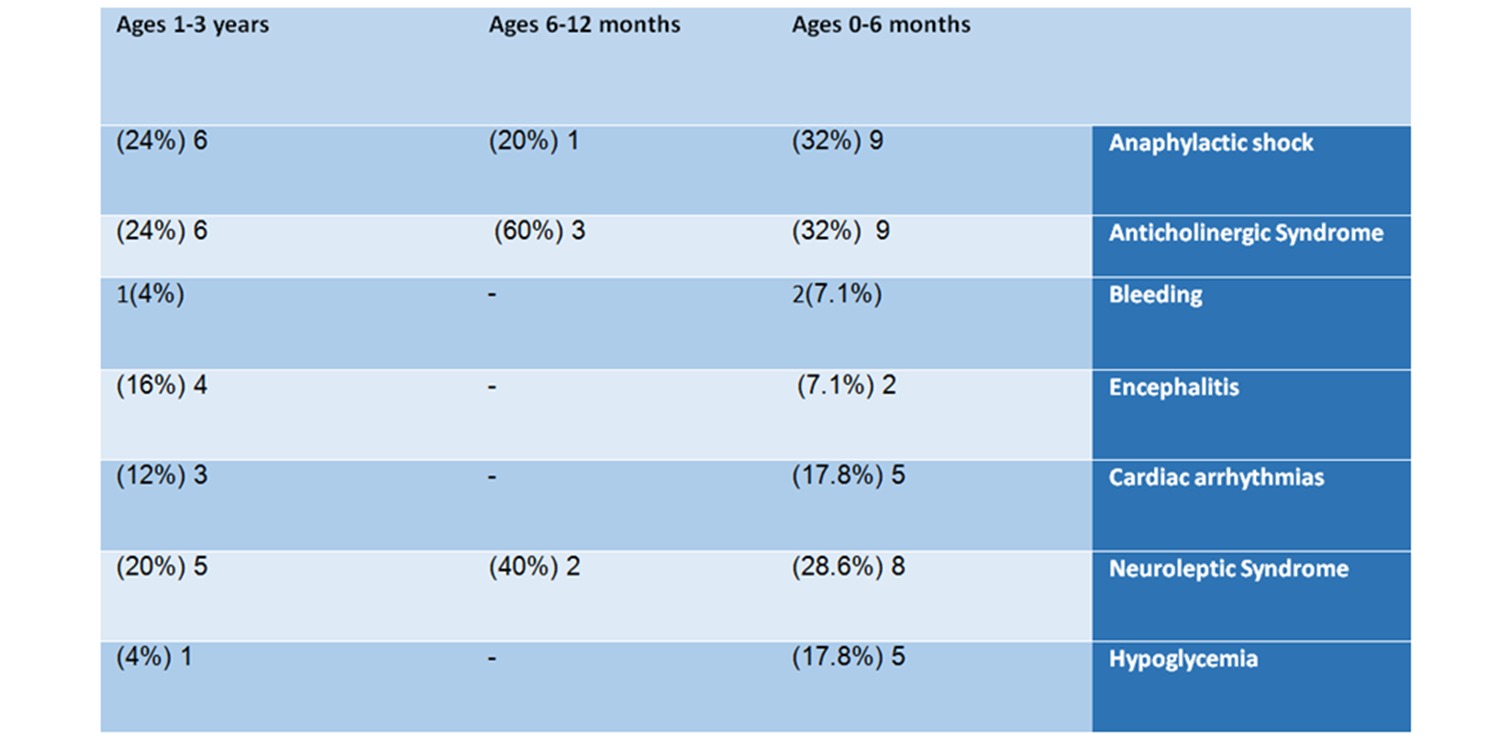
9 από αυτούς (32%) έπασχαν από αντιχολινεργικό σύνδρομο, 9 (32%) είχαν αναφυλακτικό σοκ, 8 (28,6%) έπασχαν από νευροληπτικό σύνδρομο, 5 έπασχαν από διαταραχές του καρδιακού ρυθμού και 5 είχαν υπογλυκαιμία.
Στην ηλικιακή ομάδα 6-12 μηνών – σε αυτήν την ομάδα, βρέθηκαν 5 αναφορές – 3 άνδρες, ένας θηλυκός και ένας του οποίου το φύλο δεν προσδιορίστηκε. Αυτή η ομάδα είναι μικρή σε σύγκριση με τις άλλες ομάδες. Ο κατάλογος των ανεπιθύμητων ενεργειών περιελάμβανε: αναφυλακτικό σοκ, αντιχολινεργικό σύνδρομο και νευροληπτικό σύνδρομο.
Στην ηλικιακή ομάδα ενός έως τριών ετών – σε αυτήν την ομάδα αναφέρθηκαν 25 περιπτώσεις, εκ των οποίων 5 αφορούσαν άρρενες, 19 αφορούσαν γυναίκες και ένα μωρό του οποίου το φύλο δεν προσδιορίστηκε.
6 από τα μωρά (24%) είχαν αναφυλακτικό σοκ, 6 (24%) έπασχαν από αντιχολινεργικό σύνδρομο, 5 (20%) έπασχαν από νευροληπτικό σύνδρομο, 4 (16%) έπασχαν από εγκεφαλίτιδα, 3 (12%) είχαν ακανόνιστους καρδιακούς παλμούς, ένα Το μωρό είχε αιμορραγία και το ένα έπασχε από υπογλυκαιμία.
Θα πρέπει να σημειωθεί ότι οι ανεπιθύμητες ενέργειες που αναφέρονται παραπάνω είναι μόνο μερικές από αυτές που αναφέρονται στο VAERS όσον αφορά τα μωρά. Επιλέξαμε να εστιάσουμε μόνο σε απειλητικές για τη ζωή και κοινές ανεπιθύμητες ενέργειες.
Πίνακας Νο. 1: Ανάλυση αναφορών ανά ηλικία και φύλο
Πίνακας Νο. 2: Ανάλυση αναφορών ανά ανεπιθύμητες ενέργειες
Ζουν τα μωρά;
Παρόμοια με την προηγούμενη περίπτωση που περιγράφηκε, ένα άλλο μωρό, δύο μηνών, υπέστη επίσης αναφυλακτικό σοκ μετά την έκθεση σε μία δόση του εμβολίου Pfizer-BioNTech στις 6 Ιανουαρίου 2021, και ακριβώς όπως αυτό, σύμφωνα με την έκθεση (αρ. 976433), υπέφερε από μια σειρά πολυσυστημικών συμπτωμάτων. Όσον αφορά τη μέθοδο χορήγησης του εμβολίου, αναφέρθηκε «μέσω απροσδιόριστης οδού χορήγησης» , που σημαίνει ότι δεν είναι σαφές σε ποιες συνθήκες το μωρό εκτέθηκε στο εμβόλιο.
Ήταν μέρος της κλινικής δοκιμής της Pfizers; Και πάλι, δεν είναι σαφές από την έκθεση.
Ωστόσο, το πιο σημαντικό ερώτημα που πρέπει να τεθεί, όπως και στην προηγούμενη περίπτωση, είναι τι συνέβη στο μωρό; Επιβίωσε; Είναι ζωντανή;
Και πάλι, στην ενότητα που αναφέρει το θάνατο, δηλώνει «Όχι», που σημαίνει ότι το μωρό δεν πέθανε. Ωστόσο, στην περιγραφή της αναφοράς λέει, «Ο ασθενής δεν είχε αναρρώσει από το συμβάν. Δεν είναι δυνατές προσπάθειες παρακολούθησης. Δεν αναμένονται περισσότερες πληροφορίες».
Είναι δύσκολο να πιστέψει κανείς, αλλά αυτή η βασική ερώτηση –τι συνέβη σε ένα μωρό αφού υπέστη τόσο σοβαρές και απειλητικές για τη ζωή ανεπιθύμητες ενέργειες– προκύπτει επίσης από άλλες σοβαρές περιπτώσεις, όπως η περίπτωση ενός μωρού 6 μηνών (αναφορά # 2084418 ) που «έλαβε bnt162b2 (COMIRNATY), ενδομυϊκά» στις 29 Δεκεμβρίου 2021 και πέρασε από αναφυλακτικό σοκ, αντιχολινεργικό σύνδρομο, νευροληπτικό σύνδρομο, λοιμώδη πνευμονία, άλλες λοιμώξεις και πολυσυστηματικά συμπτώματα.
In this case as well, the section reporting death states “No”, meaning supposedly the baby did not die, while in the event description it says “outcome ‘unknown’… No follow-up attempts are possible. No further information is expected”.
Σε άλλη περίπτωση (αρ. αναφοράς 1012508) ένα μωρό ενός έτους που έλαβε επίσης εμβόλιο Pfizer, στις 19 Ιανουαρίου 2021 (αυτή η περίπτωση διευκρινίζεται ότι το μωρό δεν συμμετείχε σε δοκιμή) παρουσίασε πόνο στην αριστερό αυτί που κλιμακώθηκε σε πλήρη παράλυση, η οποία διαγνώστηκε ως σύνδρομο Guillain Barre. Στην περιγραφή της υπόθεσης αναφέρθηκε ότι το μωρό έπασχε από σύνδρομο Guillain Barre, παράλυση προσώπου, μη λοιμώδη εγκεφαλίτιδα, μη λοιμώδη μηνιγγίτιδα, ωταλγίες και διαταραχές ακοής. Ωστόσο, στη σύνοψη της έκθεσης, γράφτηκε και πάλι ότι «Δεν είναι δυνατές προσπάθειες παρακολούθησης».
Και μια άλλη συγκλονιστική περίπτωση (αριθμός αναφοράς 1379484) προκύπτει από την αναφορά ενός μωρού μόλις ενός μηνός, το οποίο υπέστη «Κολπική αιμορραγία/Συνεχής βαριά κολπική αιμορραγία με κομμάτια θρόμβου» την επόμενη μέρα μετά τη λήψη του εμβολίου Pfizer-BioNTech τον Μάιο. 19, 2021.
Αν και τα συμπτώματα από τα οποία υπέφερε το μωρό ορίστηκαν ως «σοβαρά ως ιατρικά σημαντικά» , στην περιγραφή του περιστατικού αναφέρεται ότι το αποτέλεσμα είναι «άγνωστο» και ότι «Δεν είναι δυνατές προσπάθειες παρακολούθησης. Δεν αναμένονται περισσότερες πληροφορίες».
As mentioned, in some of the cases it is stated the babies were not part of a clinical trial, while in others it is not clear whether they participated in a clinical trial or were vaccinated in other unknown circumstances. But whether they were part of the trial or not, the report does not explain the absence of this critical information; what happened to these babies? Did they survive? And if so, did they recover? Why was there not a follow-up on the medical condition of babies who suffered from severe and life-threatening adverse events, while it was clearly stated that they did not recover? Is it not required in such severe cases by the FDA that the company should make every effort to locate these babies, find out what their condition is and follow up on them?
«Ερυθρότητα στην περιοχή της ένεσης: το πρωτόκολλο κλινικών δοκιμών δεν αναφέρει σοβαρές ανεπιθύμητες ενέργειες»
Το δελτίο τύπου που εκδόθηκε στις 11 Φεβρουαρίου 2022, στο οποίο η Pfizer-BioNTech ανακοίνωσε ότι σκοπεύει να υποβάλει αίτηση στον FDA για έγκριση για βρέφη από 6 μηνών έως 4 ετών, τα ευρήματα ασφάλειας από τις κλινικές δοκιμές της εταιρείας σε μωρά και νήπια σε αυτές οι ηλικίες δεν αναφέρονται ούτε με μια λέξη. Το ενημερωτικό φυλλάδιο σχετικά με τις κλινικές δοκιμές που δοκιμάζουν την ασφάλεια και την αποτελεσματικότητα του εμβολίου Pfizer σε ενήλικες, παιδιά και βρέφη, στον ιστότοπο του FDA, δηλώνει ξεκάθαρα «Δεν δημοσιεύτηκαν αποτελέσματα μελέτης στο ClinicalTrials.gov για αυτήν τη Μελέτη». Και όπως σημειώθηκε παραπάνω, το πρόσφατα δημοσιευμένο The VRBPAC Briefing Document παραθέτει μόνο μια χούφτα μη σοβαρών ανεπιθύμητων ενεργειών που αναφέρθηκαν σε αυτήν την ηλικιακή ομάδα, συμπεριλαμβανομένων και συμπεραίνει ότι δεν υπάρχει τίποτα που να υποδηλώνει νέα ανησυχία για την ασφάλεια. Πώς θα μπορούσε η FDA να μην γνωρίζει για τόσες πολλές σοβαρές ανεπιθύμητες ενέργειες που αναφέρθηκαν στα συστήματα αναφοράς του CDC; Εναλλακτικά, εάν ξέρουν για αυτά – γιατί τα αγνοούν;
Πώς ελέγχθηκαν οι ανεπιθύμητες ενέργειες σε μωρά σε σχέση με τις κλινικές δοκιμές; Σε μια προσπάθεια να απαντήσουμε σε αυτό το κρίσιμο ερώτημα, με σκοπό να αντιμετωπίσουμε τα ζητήματα ασφάλειας και να διαβεβαιώσουμε τους γονείς ότι το εμβόλιο είναι ασφαλές για τα μωρά, εξετάσαμε το πρωτόκολλο μελέτης που βρέθηκε στον ιστότοπο κλινικών δοκιμών του FDA.
Φαίνεται ότι δεν καταγράφηκαν πιθανές σοβαρές ανεπιθύμητες ενέργειες. Ο κατάλογος των πιθανών ανεπιθύμητων ενεργειών που υποτίθεται ότι θα αξιολογούσε η μελέτη σύμφωνα με το πρωτόκολλο («μέτρο έκβασης») περιελάμβανε τόσο τοπικές όσο και συστημικές αντιδράσεις. Ωστόσο, αυτές είναι σχετικά μη σοβαρές ανεπιθύμητες ενέργειες.
Ο κατάλογος των τοπικών ανεπιθύμητων ενεργειών που υποτίθεται ότι παρακολουθούσε η δοκιμή περιλαμβάνει: «Πόνος ή ευαισθησία στο σημείο της ένεσης, ερυθρότητα και οίδημα» και οι συστηματικές αντιδράσεις περιελάμβαναν «Πυρετό, κόπωση, πονοκέφαλο, ρίγη, έμετο, διάρροια, νέα ή επιδεινωμένα μυϊκός πόνος, νέος ή επιδεινωμένος πόνος στις αρθρώσεις, μειωμένη όρεξη, υπνηλία και ευερεθιστότητα». Επιπλέον, αν και η μελέτη έχει προγραμματιστεί να ολοκληρωθεί μόνο στις 14 Ιουνίου 2024, το χρονικό πλαίσιο που έχει οριστεί για την εξέταση των ανεπιθύμητων ενεργειών περιορίζεται σε επτά ημέρες μετά από κάθε δόση – την πρώτη και τη δεύτερη δόση.
Το εμβόλιο είναι αναποτελεσματικό στα βρέφη. Η λύση: χαμηλώστε το όριο αποτελεσματικότητας και προσθέστε μια τρίτη δόση
Εκτός από τις ουσιαστικές ανησυχίες σχετικά με την ασφάλεια των εμβολίων για τα μωρά, η αποτελεσματικότητά τους σε αυτήν την ηλικιακή ομάδα είναι σε μεγάλο βαθμό αμφισβητήσιμη. Σύμφωνα με τα διαθέσιμα δεδομένα, τα υγιή παιδιά διατρέχουν σχεδόν μηδενικό κίνδυνο σοβαρής ασθένειας, νοσηλείας ή θανάτου λόγω COVID-19.
Η νοσηλεία λόγω COVID-19 είναι πολύ σπάνια μεταξύ των παιδιών και οι περιπτώσεις θανάτου είναι ακόμη πιο σπάνιες. Στη Γερμανία, για παράδειγμα, μια μεγάλη μελέτη διαπίστωσε ότι ούτε ένα παιδί δεν πέθανε από COVID-19 μεταξύ 5-11 ηλικιών χωρίς προϋπάρχουσες συνθήκες. Υπό αυτές τις συνθήκες, έστω και ένα κρούσμα σοβαρού ανεπιθύμητου συμβάντος, πόσο μάλλον ο θάνατος, είναι κρίσιμο και υπερτερεί κάθε πιθανού οφέλους του εμβολίου.
Δεν αποτελεί έκπληξη το γεγονός ότι οι κλινικές δοκιμές της Pfizer σε μωρά κάτω των 4 ετών απέδειξαν ότι 2 δόσεις εμβολίου δεν αυξάνουν σημαντικά τον αριθμό των αντισωμάτων τους. Η επίτροπος του FDA, Δρ Janet Woodcock, παραδέχτηκε σε μια συνέντευξη στις αρχές Απριλίου 2022 ότι «Τα αντισώματα που αναπτύχθηκαν δεν ήταν τόσο υψηλά, επομένως δεν είχαν την ίδια απόκριση αντισωμάτων στη σειρά δύο βολών στα μεγαλύτερα παιδιά. Δεν ήταν τόσο υψηλό όσο αυτό που θα ελπίζαμε για τους νεότερους όσο για τα μεγαλύτερα παιδιά». Σύμφωνα με τον Woodcock, αυτός είναι ο λόγος που η Pfizer, η οποία σχεδίαζε να υποβάλει αίτηση για έγκριση EUA για μωρά τον Φεβρουάριο, ανέβαλε την ημερομηνία υποβολής και αποφάσισε να προσθέσει μια τρίτη δόση στη δοκιμή και να περιμένει τα ευρήματα αφού όλα τα μωρά λάβουν την τρίτη δόση τους.
Επιπλέον, σε δήλωση που δόθηκε στις 11 Μαΐου, ο Δρ Peter Marks, διευθυντής του Κέντρου Βιολογικής Αξιολόγησης και Έρευνας στο FDA, ανακοίνωσε ότι τα εμβόλια βρεφών και νηπίων δεν θα χρειαστεί να περάσουν το ποσοστό αποτελεσματικότητας 50% κατά του Covid. Ένα ποσοστό αποτελεσματικότητας 50% είναι το όριο που πρέπει να περάσουν τα εμβόλια ενηλίκων. Ωστόσο, ο Marks εξηγεί ότι παρά τις προηγούμενες κατευθυντήριες γραμμές, ο FDA δεν θα αρνηθεί τώρα την έγκριση από τις εταιρείες για μωρά και νήπια μόνο και μόνο επειδή δεν έφτασε το 50% της αποτελεσματικότητας στην πρόληψη των συμπτωματικών λοιμώξεων.
Η Pfizer εξέδωσε ένα δελτίο τύπου στις 23 Μαΐου, ανακοινώνοντας ότι «η αποτελεσματικότητα του εμβολίου 80,3% παρατηρήθηκε στην περιγραφική ανάλυση τριών δόσεων κατά τη διάρκεια μιας περιόδου που το Omicron ήταν η κυρίαρχη παραλλαγή». Σύμφωνα με το δελτίο τύπου, «Η μελέτη υποδηλώνει ότι μια χαμηλή δόση 3 μg του εμβολίου μας…, παρέχει στα μικρά παιδιά υψηλό επίπεδο προστασίας έναντι των πρόσφατων στελεχών COVID-19».
Ωστόσο, το ενημερωτικό έγγραφο του FDAαποκαλύπτει ότι ο ισχυρισμός για «υψηλό επίπεδο προστασίας» βασίζεται σε συνολικά 10 συμπτωματικές περιπτώσεις COVID-19 που εντοπίστηκαν στη δοκιμή, οι οποίες συνέβησαν τουλάχιστον 7 ημέρες μετά τη δόση 3. Τρεις από αυτές εμφανίστηκαν μεταξύ των συμμετεχόντων 6-23 μηνών ηλικία (η οποία περιελάμβανε 555 συμμετέχοντες – 376 στην ομάδα του εμβολίου και 179 στην ομάδα εικονικού φαρμάκου) – με 1 κρούσμα στην ομάδα εμβολίου Pfizer-BioNTech και δύο στην ομάδα εικονικού φαρμάκου. Επτά άλλες περιπτώσεις εμφανίστηκαν μεταξύ των συμμετεχόντων ηλικίας 2-4 ετών (οι οποίοι περιελάμβαναν 860 συμμετέχοντες – 589 στην ομάδα του εμβολίου και 271 στην ομάδα εικονικού φαρμάκου) – με 2 περιπτώσεις στην ομάδα εμβολίου Pfizer-BioNTech, σε σύγκριση με 5 στην ομάδα του εικονικού φαρμάκου. Ωστόσο, η αποτελεσματικότητα του εμβολίου πλαισιώθηκε από τον FDA ως 80,4%. και το έγγραφο καταλήγει στο συμπέρασμα ότι «Τα διαθέσιμα δεδομένα υποστηρίζουν την αποτελεσματικότητα της κύριας σειράς εμβολίων 3 δόσεων Pfizer-BioNTech COVID-19 (3 μg κάθε δόση) στην πρόληψη του COVID-19 στην ηλικιακή ομάδα 6 μηνών έως 4 ετών». Επιπλέον, το έγγραφο αναφέρει ότι «Μεταξύ βρεφών και παιδιών ηλικίας 6 μηνών έως 4 ετών, τα ποσοστά νοσηλείας και θανάτου λόγω COVID-19 είναι υψηλότερα από ό,τι μεταξύ των παιδιών και των εφήβων ηλικίας 5-17 ετών και είναι συγκρίσιμα με τα άτομα 18- 25 ετών, υπογραμμίζοντας το όφελος ενός αποτελεσματικού εμβολίου COVID19 σε αυτήν την ηλικιακή ομάδα».
Πόσο ηθικό είναι να δίνουμε σε ένα μωρό ένα εμβόλιο για μια ασθένεια που οι πιθανότητες να αρρωστήσει βαριά ή να πεθάνει είναι σχεδόν μηδενική, ενώ τα οφέλη της θεραπείας είναι ασαφή και, και οι απειλητικές για τη ζωή ανεπιθύμητες ενέργειες είναι πολύ σημαντικές;
Αυτή η ερώτηση ήταν το θέμα ενός άρθρου που δημοσιεύτηκε τον Μάρτιο του τρέχοντος έτους στο Bioethics . Οι ερευνητές δήλωσαν ότι ούτε ένας από τους κύριους ισχυρισμούς που υποστηρίζονται για να δικαιολογήσουν την έγκριση για μωρά δεν είναι έγκυρος. Σύμφωνα με αυτούς, τα οφέλη του εμβολίου για υγιή παιδιά είναι ελάχιστα και επομένως, παρόλο που οι επιπλοκές είναι σπάνιες, υπερτερούν των οφελών του εμβολίου, ειδικά επειδή δεν είναι σαφές ποιοι είναι οι βραχυπρόθεσμοι και μακροπρόθεσμοι κίνδυνοι και η εμπειρία με το εμβόλιο είναι πολύ σύντομο. Ο αλτρουιστικός ισχυρισμός της προστασίας του περιβάλλοντος είναι επίσης πολύ προβληματικός, καθώς ως εμβόλιο υπάρχει, οι ομάδες που κινδυνεύουν μπορούν να αμυνθούν και έχει ήδη αποδειχθεί ότι τα παιδιά δεν είναι οι κύριοι μεταδοτές του ιού.
Τα μέλη του Κογκρέσου απαιτούν απαντήσεις
Αυτό το ηθικό ζήτημα έχει τεθεί τις τελευταίες ημέρες από 18 μέλη του Κογκρέσου σε επιστολή που απηύθυναν στον FDA στις 7 Ιουνίου, ζητώντας απαντήσεις πριν από την απόφαση της αρχής να χορηγήσει επείγουσα άδεια για το βρεφικό εμβόλιο. Μέλη του Κογκρέσου ζήτησαν να μάθουν γιατί τα εμβόλια για τον COVID-19 είναι απαραίτητα για αυτήν την ηλικιακή ομάδα, δεδομένου ότι η ασθένεια ενέχει πολύ μικρό κίνδυνο για βρέφη και μικρά παιδιά, ότι τα εμβόλια έχουν μικρή αποτελεσματικότητα και ότι υπάρχουν πολλά αναπάντητα ερωτήματα σχετικά με ασφάλεια και ανεπιθύμητες ενέργειες αυτών των εμβολίων.
Η επιστολή παρουσιάζει 19 ερωτήσεις προς τον FDA, μεταξύ των οποίων, μεταξύ άλλων – γιατί καθυστέρησε η δημοσίευση των εκατοντάδων χιλιάδων σελίδων δεδομένων από τις μελέτες των κατασκευαστών, την κατάσταση των ανεπιθύμητων ενεργειών και πότε όλα τα δεδομένα του FDA αναμένεται να δημοσιοποιηθεί; Ζητήθηκε επίσης από τον FDA να παράσχει στο κοινό περισσότερες λεπτομέρειες σχετικά με τα παιδιά που τραυματίστηκαν σοβαρά ή πέθαναν από τον COVID-19 και πόσα παιδιά γενικά αρρώστησαν σοβαρά. Οι νομοθέτες ασχολήθηκαν επίσης με το θέμα των καρδιακών κινδύνων κατά τη χορήγηση των εμβολίων COVID-19 του mRNA σε παιδιά, σημειώνοντας ότι μετά από εμβολιασμούς που έγιναν σε μεγάλο αριθμό παιδιών ηλικίας 5-18 ετών, παρατηρήθηκε αύξηση της μυοκαρδίτιδας και της περικαρδίτιδας, με ορισμένες περιπτώσεις να καταλήγουν σε θάνατο. και οι μακροπρόθεσμες επιπτώσεις της φλεγμονής που σχετίζεται με την καρδιά που δεν έχουν ακόμη ποσοτικοποιηθεί από τις υγειονομικές αρχές. Επί πλέον,

Η FDA δεν θα μπορεί να υποστηρίξει ότι δεν γνώριζε
Όπως αναφέρθηκε, τα δεδομένα που προκύπτουν από την ανάλυση που παρουσιάζεται σε αυτό το άρθρο καταδεικνύουν πέραν πάσης αμφιβολίας ότι το εμβόλιο δεν είναι ασφαλές για μωρά και νήπια. Είτε αυτά τα παιδιά συμμετείχαν στη μελέτη είτε όχι – αυτές οι αναφορές βρίσκονται στο σύστημα VAERS εδώ και πολλούς μήνες, επομένως δεν υπάρχει περίπτωση να μην τα γνωρίζει ο FDA. Δυστυχώς, το γεγονός ότι η FDA γνώριζε τουλάχιστον μερικές από τις σοβαρές ανεπιθύμητες ενέργειες, συμπεριλαμβανομένου του αυξημένου κινδύνου νοσηρότητας τις πρώτες ημέρες μετά τον εμβολιασμό, της μυοκαρδίτιδας και του αυξημένου κινδύνου αποβολής και δυσπλασιών του εμβρύου, και ωστόσο ενέκρινε το εμβόλιο για εφήβους, παιδιά και έγκυες γυναίκες, αποκαλύφθηκε αργότερα πολύ αργά – πολύ μετά τη χορήγηση του EUA στην Pfizer και τη Moderna, όταν πολλοί έχουν ήδη πληγεί. Έγινε σαφές μόνο χάρη στα αιτήματα FOIA (Ελευθερία της Πληροφορίας) που υποβλήθηκαν στην FDA και σε άλλες υγειονομικές αρχές, και μόνο αφού η FDA αναγκάστηκε από το δικαστήριο να αποκαλύψει τα έγγραφα. Αυτή τη φορά, τα δεδομένα της VAERS που παρουσιάζονται εδώ καθιστούν δυνατή την αποκάλυψη αυτού του γεγονότος ακόμη και πριν από την έγκριση. Η FDA δεν θα μπορεί να ισχυριστεί ότι δεν γνώριζε.
Σημείωση για τους αναγνώστες: Κάντε κλικ στα κουμπιά κοινής χρήσης πάνω ή κάτω. Ακολουθήστε μας στο Instagram και στο Twitter και εγγραφείτε στο κανάλι μας στο Telegram. Μη διστάσετε να αναδημοσιεύσετε και να μοιραστείτε ευρέως άρθρα της Παγκόσμιας Έρευνας.
Η επιλεγμένη εικόνα είναι από το περιοδικό Real Time